Le concept de biocompatibilité fait référence à l’interaction entre les tissus et les systèmes physiologiques d’un patient traité avec un dispositif médical. L’évaluation de la biocompatibilité fait partie de l’évaluation globale de la sécurité du dispositif.
L’évaluation de la biocompatibilité des dispositifs médicaux est en fait réalisée afin de garantir la sécurité des patients. Lors de la programmation d’un test de biocompatibilité, les fabricants doivent tenir compte de leurs objectifs de conformité et des risques. En fait, l’évaluation de la biocompatibilité des dispositifs médicaux est une étude d’évaluation des risques. Tous les dispositifs médicaux présentent un certain niveau de risque. Les entreprises qui conçoivent des dispositifs médicaux s’efforcent de maximiser les avantages qu’ils procurent aux patients en minimisant les risques.
La principale norme en matière d’essais de biocompatibilité est la norme ISO 10993 normes. La première partie de cette norme est le guide de sélection des essais. Les sections suivantes couvrent les processus d’essai spécifiques et d’autres considérations liées à l’essai.
Les données relatives aux essais de biocompatibilité sont toujours nécessaires pour les dispositifs ayant un contact important avec les tissus. La matrice de biocompatibilité des matériaux de l’ISO 10993-1 est utilisée pour déterminer si un dispositif médical nécessite un essai de biocompatibilité. ISO 10993-1 : 2018 par le biais de la Plan d’évaluation biologique (PEB) permet de déterminer le risque potentiel sur la base des données fournies par le promoteur (informations sur les matières premières, l’emballage, les conditions de production et les études réalisées antérieurement). L’étape suivante consiste en une série d’études proposées dans le MPE pour vérifier les évaluations des risques, et enfin dans le Rapport d’évaluation biologique (BER) L’évaluation des risques est résumée et les sources potentielles de non-conformité sont expliquées.

Dans toutes les régions du monde, les fabricants de dispositifs médicaux sont tenus de prouver les performances de leurs produits en matière de biocompatibilité. Dans certains pays (Chine, États-Unis, Canada), les exigences en matière de tests de biocompatibilité peuvent être différentes. Si le fabricant conserve les données des livraisons précédentes, les données des fournisseurs de matériaux ou de composants, les données analytiques et les données cliniques, le nombre de tests est légèrement réduit.
L’objectif principal de la norme ISO est de vérifier que le dispositif est adapté à l’utilisation prévue. Dans ce processus, les tests biologiques constituent l’étape la plus importante de l’évaluation de la biocompatibilité. La norme classe les dispositifs en fonction du type de contact avec le corps et de la durée.
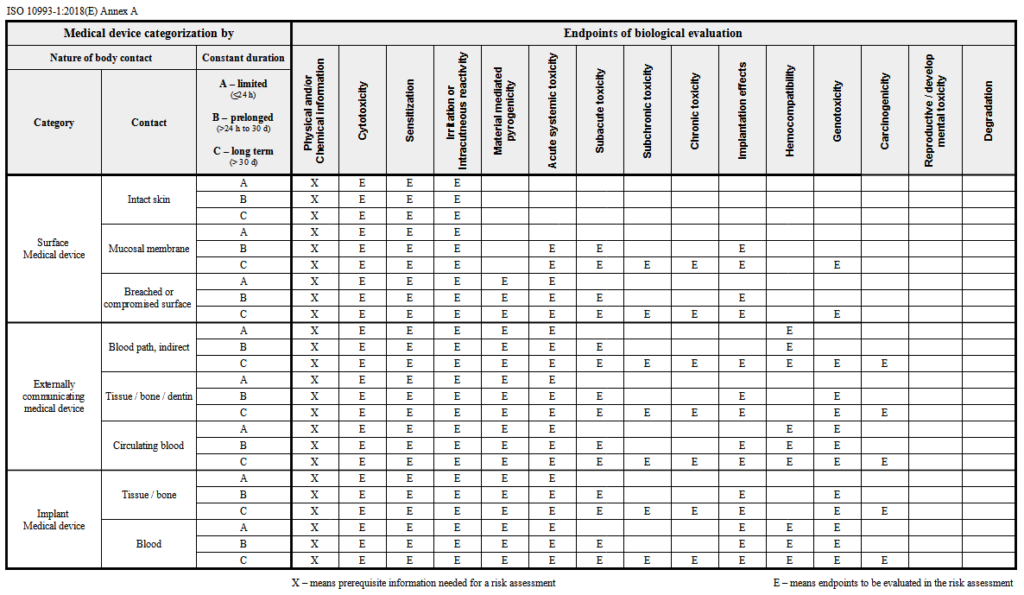
La biocompatibilité est souvent associée à la nécessité d’effectuer une série complète de tests pour les nouveaux dispositifs médicaux qui n’ont pas encore été mis sur le marché. Mais les fabricants de dispositifs médicaux ne doivent pas oublier que, parfois, un changement apparemment minime dans le processus de production de produits déjà disponibles sur le marché (par exemple : changement d’un des matériaux, changement de la méthode de production, introduction de nouvelles machines dans la chaîne de production, ou un changement apparemment insignifiant dans la méthode de stérilisation) est associé à une autre évaluation des risques et à la réalisation d’essais de biocompatibilité. Les fabricants sont également tenus de collecter des données de sécurité pour tous les composants et matériaux utilisés dans les dispositifs médicaux.
L’Institut biomédical européen est certifié Bonnes pratiques de laboratoire (BPL) et accrédité ISO 17025. Notre société fournit également des services d’essais de biocompatibilité dans le domaine des services de certification. Grâce à ces services, les entreprises sont en mesure de fabriquer des produits plus efficaces, plus performants et de meilleure qualité, de manière sûre, rapide et ininterrompue.
Pour de plus amples informations, veuillez contacter votre représentant commercial si vous êtes un client existant ou si vous êtes un nouveau client. Institut biomédical européen, veuillez nous contacter à l’adresse suivante contact@ebi.bio ou visitez notre site web https://ebi.bio/
Nous sommes impatients de vous aider à atteindre tous vos objectifs d’évaluation et à réussir votre soumission !
Nous sommes là pour vous soutenir !